伴随着肥胖、糖尿病以及代谢综合征的大量增加,MASH(代谢失调相关脂肪性肝炎)相关HCC(MASH-HCC)发病率呈现快速上升的趋势,每年约有2%的人从MASH进展到MASH-HCC,对全球公众健康构成了严重的威胁。与其他病因HCC相比,MASH-HCC具有独特的分子、免疫特征以及治疗响应。从MASH进展到MASH-HCC的具体机制目前尚不明确,其可能受到多种因素的影响,包括组织和免疫微环境,基因突变和微生物组等,阐明其内在的分子机制是克服MASH-HCC疗效不佳难题的主要突破口之一,具有重要的研究意义和临床应用前景。
2025 年 10 月 16 日,国家肝癌科学中心、东方肝胆外科医院王红阳院士、李亮教授共同通讯,付靖波、危晏平等共同第一作者在Cancer Communications(IF=24.9)在线发表题为“Intranuclear paraspeckle-circular RNA TACC3 assemblyforms RNA-DNA hybrids to facilitateMASH-relatedhepatocellular carcinoma growth in anm6A-dependentmanner”的研究论文,发现circRNA-DNA互作失调是连接代谢应激、表观遗传修饰与MASH-HCC进展的关键分子桥梁。
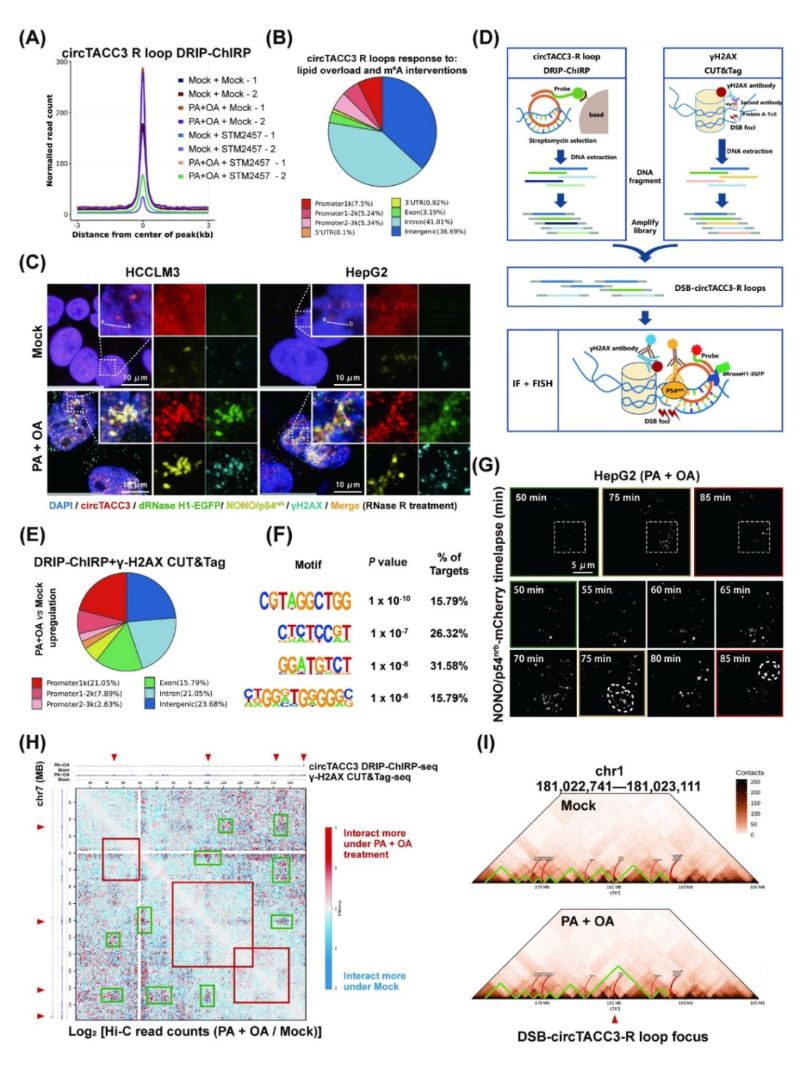
研究指出,脂质应激条件下,依赖于m⁶A RNA甲基化修饰的环状circTACC3-paraspeckle(旁斑)结构组装可以在DNA双链断裂点区域形成circRNA-DNA杂交体(CircR loops),从而导致染色质重塑、并选择性激活与MASH-HCC恶性进展相关的基因。这一新的机制发现为潜在的MASH-HCC治疗靶点提供了依据。
据估算,中国、法国、德国、意大利、日本、西班牙、英国和美国的MASH患病率至2030年将增长高至56%;目前西方国家MASH相关HCC约占HCC总病例的20%,预计至2030年MASH将成为全球HCC的主要病因。目前,中国的MASLD(代谢失调相关脂肪性肝病)患者约2.5亿人,已经高于现有HBV(hepatitis B virus)携带者人数;根据现有数据预测,2030年中国MASLD患者可达3亿人,其中15%可能进展至MASH,而MASH-HCC发病可能达到30万人/年,防控形势异常严峻。
从发病率来说,MASH-HCC男性和女性同样普遍。早期到中期的MASH-HCC一般可以进行手术和局部治疗;但是,与MASH相关的并发症比如肥胖和2型糖尿病,可以严重影响某些患者实施潜在的治愈性治疗的疗效。晚期MASH-HCC采用全身治疗,比如抗血管生成治疗和免疫检查点抑制剂;但是,不同的微环境因素可能限制MASH-HCC对免疫治疗的反应。研究数据表明MASH-HCC与病毒相关HCC相比有着更差的免疫治疗效果, 最近的研究发现由于CD8+PD1+T细胞的功能失调性浸润,MASH-HCC对免疫检查点抑制剂(immune checkpoint inhibitors, ICI)的反应较低,这些发现与肥胖诱导肿瘤微环境代谢变化导致CD8+T细胞损伤的观察结果一致。
RNA修饰的发现为真核生物的基因表达调控及功能研究开辟了一个全新的领域,表观转录组(epitranscriptomics)的研究近年来成为医学、生物学研究的前沿热点之一。该课题组利用表观转录组芯片筛选了MASH-HCC肿瘤与癌旁组织对比的m6A修饰circRNAs指纹图谱,发现一种尚未被功能验证过的circRNA:Circ-TACC3(hsa_circRNA _406433)是MASH-HCC中表达丰度高且m6A修饰最显著的circRNA。MASH病程中脂质过载会导致DNA双链断裂及DNA损伤反应,进一步的,该课题组发现这种细胞反应可能诱导Circ-TACC3发生m6A RNA甲基化修;m6A甲基化修饰通过特定的途径促进Circ-TACC3与细胞核内NONO/P54nrb蛋白、lncNEAT1等形成一种亚核结构旁斑(paraspeckle);旁斑有助于保持外显子来源的Circ-TACC3的核内驻留。已知旁斑及NONO/P54nrb蛋白可被诱导参与DNA损伤修复反应,因此可携带Circ-TACC3向基因组损伤区域靠近并形成DNA-circRNA杂交结构CircR loops;Circ-TACC3相关CircR loops通过参与DNA损伤反应等机制影响基因组结构重塑以及MASH-HCC相关基因的选择性激活,并正反馈促进其旁斑的形成。在这种DNA损伤反应-Circ-TACC3 m6A修饰-旁斑形成、Circ-TACC3核驻留-CircR loops形成-基因组结构重塑、基因激活-旁斑形成的正反馈循环反复作用下,肝细胞染色质重塑以及损伤反应、肿瘤相关的一系列关键基因表达失调,最终促进MASH-HCC的进展。
图1(图源自Cancer Communications)
这一研究发现,有望为阐明MASH-HCC的独特临床表现提供新的理论认识。本研究还研发了 DRIP-ChiRP技术,创新性实现对特定circRNA(如Circ-TACC3)形成的R-loops结构进行全基因组捕获与功能解析。该技术可精准筛选脂质过载及m⁶A修饰对Circ-TACC3-R-loops的调控靶点,结合染色质构象与下游致癌通路分析,为MASH-HCC提供机制发现-靶点筛选-干预策略的一体化研究体系,有望推动基于RNA-DNA互作精准干预的转化医学实践。
原文链接:
https://onlinelibrary.wiley.com/doi/10.1002/cac2.70061
(来源:iNature)
最新动态
-
 2022-01-04
2022-01-04
-
 2021-10-20
2021-10-20
-
科技部等十三部门印发《关于支持女性科技人才在科技创新中发挥更大作用的若...
 2021-07-30
2021-07-30
-
 2021-07-19
2021-07-19
-
 2021-07-19
2021-07-19
精彩视频
-

 2021-11-29
2021-11-29
-

 2021-11-29
2021-11-29